Структура сульфида серебра (Ag2S), свойства, номенклатура, применение
сульфид серебра неорганическое соединение, чья химическая формула Ag2S. Он состоит из черно-сероватого твердого вещества, образованного катионами Ag+ и анионы S2- в соотношении 2: 1. S2- это очень похоже на Ag+, потому что оба являются мягкими ионами, и им удается стабилизироваться друг с другом.
Серебряные украшения имеют тенденцию темнеть, теряя свой характерный блеск. Изменение цвета является не продуктом окисления серебра, а его реакции с сероводородом, присутствующим в окружающей среде при низких концентрациях; Это может происходить из-за гниения или деградации растений, животных или продуктов, богатых серой..

H2S, чья молекула несет атом серы, реагирует с серебром в соответствии со следующим химическим уравнением: 2Ag (s) + H2S (g) => Ag2S (s) + H2(G)
Следовательно, Ag2S отвечает за черные слои, сформированные на серебре. Однако в природе эту серу также можно найти в минералах acantita и argentita. Эти два минерала отличаются от многих других своими черными и яркими кристаллами, как у твердого вещества на верхнем изображении..
Ag2S представляет полиморфные структуры, привлекательные электронные и оптоэлектронные свойства, является полупроводниковым и обещает стать материалом для разработки фотоэлектрических устройств, таких как солнечные элементы.
индекс
- 1 структура
- 2 свойства
- 2.1 Молекулярный вес
- 2.2 Внешний вид
- 2.3 Запах
- 2.4 Точка плавления
- 2.5 Растворимость
- 2.6 Структура
- 2.7 Показатель преломления
- 2.8 Диэлектрическая проницаемость
- 2.9 Электроника
- 2.10 Реакция восстановления
- 3 Номенклатура
- 3.1 Систематика
- 3.2 Сток
- 3.3 Традиционный
- 4 использования
- 5 ссылок
структура
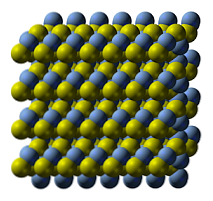
Кристаллическая структура сульфида серебра показана на верхнем изображении. Синие сферы соответствуют катионам Ag+, в то время как желтые анионы S2-. Ag2S является полиморфным, что означает, что он может принимать несколько кристаллических систем при определенных температурных условиях.
Как? Через фазовый переход. Ионы переставляются таким образом, что повышение температуры и колебания твердого тела не нарушают электростатического равновесия притяжения-отталкивания. Когда это происходит, говорят, что существует фазовый переход, и поэтому твердое тело проявляет новые физические свойства (такие как блеск и цвет)..
Ag2S при нормальной температуре (ниже 179ºC), он имеет моноклинную кристаллическую структуру (α-Ag2S). Помимо этой твердой фазы есть еще две: ОЦК (кубический с центром в теле) между 179 и 586ºC, и ГЦК (кубический с центром на гранях) при очень высоких температурах (δ-Ag2S).
Минерал аргентита состоит из ГЦК-фазы, также известной как β-Ag2S. После охлаждения и превращения в скалы, их структурные особенности преобладают вместе. Следовательно, обе кристаллические структуры сосуществуют: моноклинная и ОЦК. Следовательно, черные тела с яркими и интересными оттенками появляются.
свойства
Молекулярный вес
247.80 г / моль
внешний вид
Серовато-черные кристаллы
запах
туалет.
Точка плавления
836ºC. Эта величина согласуется с тем, что Ag2S представляет собой соединение с небольшим ионным характером и, следовательно, плавится при температуре ниже 1000ºC.
растворимость
В воде всего 6,21 ∙ 10-15 г / л при 25ºC. То есть количество черного твердого вещества, которое растворяется, незначительно. Это, опять же, связано с небольшим полярным характером связи Ag-S, где нет существенной разницы в электроотрицательности между обоими атомами.
Кроме того, Ag2S нерастворим во всех растворителях. Ни одна молекула не может эффективно отделить свои кристаллические слои от ионов Ag+ и S2- сольватирован.
структура
На изображении структуры также видны четыре слоя связей S-Ag-S, которые движутся друг над другом, когда твердое тело подвергается пониманию. Такое поведение означает, что, несмотря на то, что он является полупроводником, он пластичен, как и многие металлы при комнатной температуре..
Слои S-Ag-S подходят правильно из-за их угловой геометрии, которые наблюдаются как зигзаг. Обладая силой понимания, они движутся по оси смещения, вызывая новые нековалентные взаимодействия между атомами серебра и серы..
Показатель преломления
2,2
Диэлектрическая проницаемость
6
электронный
Ag2S - амфотерный полупроводник, то есть он ведет себя так, как если бы он был N и типа р. Он также не хрупкий, поэтому его изучали для применения в электронных устройствах..
Редукционная реакция
Ag2S можно уменьшить до металлического серебра, облив черные кусочки горячей водой, NaOH, алюминием и солью. Происходит следующая реакция:
3AG2S (s) + 2Al (s) + 3H2O (l) => 6Ag (s) + 3H2S (ac) + Al2О3(S),
номенклатура
Серебро, чья электронная конфигурация [Kr] 4d105S1, он может потерять только один электрон: тот, что находится на его самой внешней орбите 5 с. Таким образом, Ag катион+ остается с электронной конфигурацией [Kr] 4d10. Следовательно, он имеет уникальную валентность +1, которая определяет, как его соединения следует называть.
Сера, с другой стороны, имеет электронную конфигурацию [Ne] 3s23p4, и ему нужно два электрона для завершения своего валентного октета. Когда он получает эти два электрона (из серебра), он превращается в анион серы, S2-, с конфигурацией [Ar]. То есть это изоэлектронный благородный газ аргона.
Так что Ag2S следует называть в соответствии со следующими номенклатурами:
Систематика
обезьянасульфид дисеребро. Здесь мы рассмотрим количество атомов каждого элемента и обозначены префиксами греческих числителей.
акции
Сульфид серебра. При уникальной валентности +1 она не указывается римскими цифрами в скобках: сульфид серебра (I); что неверно.
традиционный
Sulfuro argéntICO. Поскольку серебро «работает» с валентностью +1, к его имени добавляется суффикс -ico. Argentum на латыни.
приложений
Некоторые из новых применений Ag2S следующие:
-Растворы окраски их наночастиц (с различными размерами), обладают антибактериальной активностью, не токсичны, и, следовательно, могут быть использованы в областях медицины и биологии.
-Их наночастицы могут образовывать так называемые квантовые точки. Они поглощают и испускают излучение с большей интенсивностью, чем многие органические флуоресцентные молекулы, поэтому они могут вытеснить последние в качестве биологических маркеров.
-Структуры α-Ag2S заставляют его проявлять поразительные электронные свойства для использования в качестве солнечных элементов. Он также представляет собой отправную точку для синтеза новых термоэлектрических материалов и датчиков.
ссылки
- Марк Пеплоу. (17 апреля 2018 г.) Полупроводниковый сульфид серебра растягивается как металл. Взято из: cen.acs.org
- Сотрудничество: Авторы и редакторы тома III / 17E-17F-41C () Кристаллическая структура сульфида серебра (Ag2S). В: Маделунг О., Рёсслер У., Шульц М. (ред.) Нететраэдрически связанные элементы и бинарные соединения I. Ландольт-Бёрнштейн - конденсированная среда III группы (числовые данные и функциональные связи в науке и технике), том 41C. Спрингер, Берлин, Гейдельберг.
- Wikipedia. (2018). Сульфид серебра. Взято из: en.wikipedia.org
- Станислав Иванович Садовников и кол. (Июль 2016 г.) Ag2Наночастицы и коллоидные растворы сульфида серебра: синтез и свойства. Взято из: sciencedirect.com
- Азо Материалы. (2018). Сульфид серебра (Ag2S) Полупроводники. Взято из: azom.com
- А. Нвофе. (2015). Перспективы и проблемы тонких пленок сульфида серебра: обзор. Отдел материаловедения и возобновляемых источников энергии, факультет промышленной физики, Государственный университет Эбони, Абакалики, Нигерия.
- UMassAmherst. (2011). Демонстрация лекций: чистка потускневшего серебра. Взято из: lecturedemos.chem.umass.edu
- Исследование. (2018). Что такое сульфид серебра? - Химическая формула и использование. Взято из: study.com


