Сульфид алюминия (Al2S3) Химическая структура, номенклатура, свойства
сульфид алюминия (Al2S3) представляет собой светло-серое химическое соединение, образованное в результате окисления металлического алюминия путем потери электронов последнего энергетического уровня и превращения в катион, а также из-за восстановления неметаллической серы путем завоевания электронов, образующихся из алюминия и превращения в анион.
Чтобы это произошло и алюминий мог дать свои электроны, необходимо представить три гибридных орбитальных sp3, которые дают возможность образования связей с электронами из серы.

Чувствительность сульфида алюминия к воде означает, что в присутствии водяного пара в воздухе он может вступать в реакцию с образованием гидроксида алюминия (Al (OH)).3), сероводород (H2S) и водород (H2) Газ; если последний накапливается, это может вызвать взрыв. Поэтому упаковка сульфида алюминия должна производиться с использованием герметичных контейнеров.
С другой стороны, поскольку сульфид алюминия имеет реакционную способность с водой, это делает его элементом, который не имеет растворимости в указанном растворителе..
индекс
- 1 Химическая структура
- 1.1 Молекулярная формула
- 1.2 Структурная формула
- 2 свойства
- 2.1 Физические свойства
- 2.2 Химические свойства
- 3 Использование и применение
- 3.1 В суперконденсаторах
- 3.2 Во вторичных литиевых батареях
- 4 риска
- 4.1 Процедура оказания первой помощи
- 4.2 Противопожарные меры
- 5 ссылок
Химическая структура
Молекулярная формула
в2S3
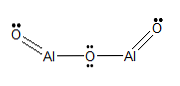
Структурная формула
- Сульфид алюминия.
- Ди трисульфид алюминия.
- Сульфид алюминия (III).
- Сульфид алюминия.
свойства
Химические соединения в основном проявляют два вида свойств: физические и химические.
Физические свойства
Молярная масса
150 158 г / моль
плотность
2,02 г / мл
Точка плавления
1100 ° С
Растворимость в воде
неразрешимый
Химические свойства
Одной из основных реакций сульфида алюминия является вода в качестве субстрата или основного реагента:

В этой реакции может наблюдаться образование гидроксида алюминия и сероводорода, если он находится в форме газа, или сероводорода, если он растворяется в воде в виде раствора. Его присутствие определяется запахом тухлых яиц.
Использование и приложения
В суперконденсаторах
Сульфид алюминия используется в производстве наносеточных структур, которые улучшают удельную площадь поверхности и электрическую проводимость таким образом, что могут быть достигнуты высокая емкость и плотность энергии, применимость которых применима для суперконденсаторов..
Оксид графена (GO) - графен является одной из аллотропных форм углерода - служил основой для сульфида алюминия (Al2S3) с иерархической морфологией, сходной с таковой у наномонтана, изготовленного с использованием гидротермального метода.
Действие оксида графена
Характеристики оксида графена в качестве носителя, а также высокая электропроводность и площадь поверхности делают нанорамбант Al2S3 быть электрохимически активным.
Кривые удельной емкости CV с четко определенными окислительно-восстановительными пиками подтверждают псевдо-емкостное поведение нанорамбутанов Al2S3 иерархическая, поддерживается в оксиде графена в 1М электролите NaOH. Значения удельной емкости CV, полученные из кривых: 168,97 при скорости сканирования 5 мВ / с..
Кроме того, наблюдалось хорошее время гальваностатического разряда 903 мкс, большая удельная емкость 2178,16 при плотности тока 3 мА / см.2. Плотность энергии, рассчитанная по гальваностатическому разряду, составляет 108,91 Втч / кг при плотности тока 3 мА / см.2.
Таким образом, электрохимический импеданс подтверждает псевдо-емкостную природу иерархического наногуммирующего электрода Al.2S3. Испытание на стабильность электрода показывает сохранение удельной емкости на 57,44% до 1000 циклов.
Результаты экспериментов свидетельствуют о том, что нанорамбутант Al2S3 Иерархический подходит для приложений суперконденсаторов.
Во вторичных литиевых батареях
С целью разработки литиевой вторичной батареи с высокой плотностью энергии, сульфид алюминия (Al2S3) в качестве активного материала.
Начальная разрядная емкость измеряется от Al2S3 было приблизительно 1170 мАч г-1 при 100 мА г-1. Это соответствует 62% теоретической емкости по сере.
Аль2S3 проявлял слабое удержание емкости в диапазоне потенциалов между 0,01 В и 2,0 В, главным образом из-за структурной необратимости процесса зарядки или извлечения Li..
Анализ XRD и K-XANES для алюминия и серы показал, что поверхность Al2S3 обратимо реагирует во время процессов загрузки и выгрузки, в то время как ядро Al2S3 показал структурную необратимость, потому что LiAl и Li2S были сформированы из Al2S3 в начальной загрузке, а затем они остались, как они были.
риски
- При соприкосновении с водой выделяет легковоспламеняющиеся газы, которые могут самовозгораться.
- Вызывает раздражение кожи.
- Вызывает серьезное раздражение глаз.
- Может вызвать раздражение дыхательных путей.
Информация может варьироваться между уведомлениями в зависимости от примесей, добавок и других факторов.
Первая помощь
Общее лечение
Обратиться к врачу, если симптомы не проходят.
Специальное лечение
никто
Важные симптомы
никто
ингаляция
Выведите жертву на улицу. Подача кислорода при затрудненном дыхании.
прием пищи
Администрирование один или два стакана воды и вызвать рвоту. Никогда не вызывайте рвоту и не дайте что-либо в рот человеку без сознания.
кожа
Промойте пораженный участок водой и мягким мылом. Удалить всю загрязненную одежду.
глаза
Вымойте глаза водой, часто мигая в течение нескольких минут. Снимите контактные линзы, если они есть, и продолжайте промывать.
Противопожарные меры
воспламеняемость
Не горючий.
Средства пожаротушения
Реагирует с водой. Не используйте воду: используйте CO2, песок и порошок для тушения.
Боевая процедура
Используйте автономный дыхательный аппарат с полной защитой лица. Носите одежду, чтобы избежать контакта с кожей и глазами.
ссылки
- Salud y Riesgos.com, (s.f), Определение, концепции и статьи о здоровье, рисках и окружающей среде. Восстановлено: saludyriesgos.com
- Сульфид алюминия. (S.f). На викиванде. Получено 9 марта 2018 года: wikiwand.com
- Веб-элементы. (S.f). Диалюминий трисульфид, восстановленный 10 марта 2018 года: webelements.com
- Икбал М., Хасан М., М., Биби С., Парвин Б. (2017). Высокая удельная емкость и энергетическая плотность синтезированного на основе оксида графена иерархического нанорамбутана Al2S3 для применения в суперконденсаторах, Электрохимия Acta, Том 246 ,Страницы 1097-1103
- Сено, Х., Такеучи, Т., Хироюки, К., Сакабе, Х., М., Наканиси, К., Охта, Т., Сакаи, Т., Ясуда, К. (2010). Электрохимические характеристики сульфида алюминия для использования в литии.Журнал источников энергии,Том 195, Выпуск 24, стр. 8327-8330 doi.org
- LTS Research Laboratories, Inc (2016), паспорт безопасности. Сульфид алюминия: ltschem.com