Химическое строение, свойства и применение сульфата аммония
сульфат аммония Это тройная и аммиачная неорганическая соль серной кислоты. Его химическая формула (NH4)2SW4. Поэтому стехиометрические пропорции говорят о том, что для каждого сульфат-аниона есть два катиона аммония, взаимодействующих с ним. Это позволяет нейтральность соли ((+1) + 2 + (-2)).
Его номенклатура обусловлена тем, что это соль, полученная из H2SW4, изменив суффикс "uric" на "ato". Таким образом, два начальных протона заменены на NH4+, продукт реакции с аммиаком (NH3). Тогда химическое уравнение для его синтеза имеет вид: 2 NH3 + H2SW4 => (NH4)2SW4
Сульфат аммония является хранилищем азота и серы, которые необходимы в химии почв и удобрений.
индекс
- 1 Химическая структура
- 2 Физические и химические свойства
- 2.1 Молекулярный вес
- 2.2 Внешний вид
- 2.3 Запах
- 2.4 Точка плавления
- 2.5 Растворимость
- 2.6 Плотность
- 2.7 Давление пара
- 2.8 Температура вспышки
- 2,9 рН
- 2.10 Стабильность
- 2.11 Разложение
- 2.12 Коррозия
- 3 использования
- 3.1 В сельском хозяйстве
- 3.2 В качестве аналитического реагента
- 3.3 В осаждении и выделении белков
- 3.4 В отрасли
- 3.5 Другое использование
- 4 Ссылки
Химическая структура
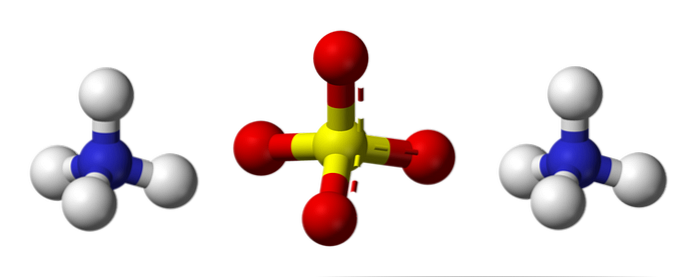
Верхнее изображение иллюстрирует молекулярную геометрию ионов NH4+ и так42-. Красные сферы соответствуют атомам кислорода, белые сферы соответствуют атомам водорода, синие сферы - атому азота, а желтые сферы - атому серы..
Оба иона можно рассматривать как два тетраэдра, и, таким образом, они имеют три единицы, которые взаимодействуют друг с другом, образуя ромбическую кристаллическую структуру. Сульфат-анион является SO42- и может пожертвовать или принять четыре водородные связи, так же, как катион NH4+.
Физико-химические свойства
Молекулярный вес
132 134 г / моль.
Внешний вид
Сплошной белый. Орторомбические белые или коричневые кристаллы, в зависимости от уровня примесей.
запах
туалет.
Точка плавления
280 ºC. Эта температура плавления, низкая по сравнению с другими ионными соединениями, обусловлена тем фактом, что это соль с одновалентными катионами (+1) и разнородными ионами по своим размерам, в результате чего твердое вещество имеет низкую кристаллическую ретикулярную энергию.
растворимость
76,4 г / 100 г воды при 25 ºC. Это сродство к воде обусловлено большой способностью ее молекул сольватировать ионы аммония. С другой стороны, он нерастворим в ацетоне и спирте; то есть в растворителях менее полярных, чем вода.
плотность
1,77 г / см3 при 25 ºC.
Давление пара
1871 кПа при 20 ºC.
Точка воспламенения
26 ºC.
pH
5,0-6,0 (25 ° С, 1 М раствор). Слабокислотный рН обусловлен гидролизом NH4+ в воде, производя H3О+ в низких концентрациях.
стабильность
Стабильно в подходящих условиях окружающей среды. При контакте с сильными окислителями может загореться.
разложение
Он начинает разлагаться при 150 ºC, выделяя токсичные пары оксида серы, оксида азота и аммония.
коррозия
Не атакует железо или алюминий.
приложений

В сельском хозяйстве
- Сульфат аммония используется в качестве удобрения на щелочных почвах. Соль аммония имеет 21% азота и 24% серы в своем составе. Однако существуют соединения, которые обеспечивают большее количество азота, чем сульфат аммония; Преимуществом последнего является его высокая концентрация серы.
- Сера необходима для синтеза белков, поскольку некоторые аминокислоты, такие как цистин, метионин и цистеин, содержат серу. По этим причинам сульфат аммония продолжает оставаться одним из наиболее важных удобрений..
- Используется в посевах пшеницы, кукурузы, риса, хлопка, картофеля, конопли и фруктовых деревьев..
- Низкий pH щелочных почв из-за их вклада в процесс нитрификации, осуществляемый микробами. Аммоний (NH) используется4+) для производства нитрата (НЕТ3-) и выпустить H+: 2NH4+ + 4О2 => 2НЕТ3- + 2H2O + 4H+. Увеличение концентрации водорода снижает рН щелочных почв и позволяет больше использовать.
- Помимо использования в качестве удобрения, сульфат аммония действует как вспомогательное средство для растворимых инсектицидов, гербицидов и фунгицидов, которые распыляются на сельскохозяйственные культуры..
- Сульфат способен улавливать ионы, присутствующие в почве и в поливной воде, которые необходимы для жизни определенных патогенных микроорганизмов. Среди ионов, которые захватывает сульфат аммония, Ca2+, Mg2+, вера2+ и вера3+. Это действие усиливает микробицидное действие указанных агентов..
В качестве аналитического реагента
Сульфат аммония действует как осаждающий агент в электрохимическом анализе, в микробиологических питательных средах и при получении солей аммония.
В осаждении и выделении белков
Сульфат аммония используется для выделения и очистки белков, особенно белков плазмы. Количество сульфата аммония добавляют в плазму до определенной концентрации; таким образом, осаждение группы белков вызвано.
Осадок собирают центрифугированием, и к супернатанту добавляют дополнительное количество сульфата аммония, и при новой концентрации происходит осаждение другой группы белков..
Повторение предыдущего процесса в последовательной форме позволяет в результате получать разные фракции белков плазмы..
До появления новых технологий молекулярной биологии эта процедура позволила выделить белки плазмы, имеющие большое значение в медицине, например: иммуноглобулины, факторы свертывания крови и т. Д..
В промышленности
Сульфат аммония действует, чтобы замедлить начало пожара в текстильной промышленности. Используется в качестве добавки в гальванической промышленности. Он также используется в производстве перекиси водорода, хлорида аммония и т. Д..
Другое использование
- Сульфат аммония используется в качестве регулирующего агента осмотического давления и в качестве осадителя соли.
- В форме лаурилсульфата аммония поверхностное натяжение воды уменьшается, что позволяет отделить загрязняющие вещества за счет повышения жесткости воды.
- Это антикоррозионный агент.
- Используется в качестве пищевой добавки, которая регулирует кислотность в мучном тесте и хлебе..
ссылки
- МОРГ ОЭСР. (Октябрь 2004 г.) Сульфат аммония. [PDF]. Получено 27 апреля 2018 г. с сайта inchem.org
- Мозаичная Компания. (2018). Сульфат аммония. Получено 27 апреля 2018 г. из: cropnutrition.com
- Wikipedia. (2018). Сульфат аммония. Получено 27 апреля 2018 г. с сайта en.wikipedia.org
- PubChem. (2018). Сульфат аммония. Получено 27 апреля 2018 г. из: pubchem.ncbi.nlm.nih.gov UpSticksNGo Crew.
- (23 июля 2015 г.) [Рисунок]. Получено 27 апреля 2018 г. с сайта: flickr.com
- Паула Папп (22 февраля 2017 г.) Применение и использование сульфата аммония. Получено 27 апреля 2018 г. из: business.com


