Хлорид олова (SnCl2) свойства, структура, использование и риски
хлорид олова (II) или хлорид олова, химической формулы SnCl2, представляет собой белое кристаллическое твердое соединение, продукт реакции олова и концентрированного раствора соляной кислоты: Sn (s) + 2HCl (конц) => SnCl2(вод) + H2(G). Процесс его синтеза (приготовления) состоит из добавления кусочков оловянных опилок для взаимодействия с кислотой.
После добавления кусочков олова происходит дегидратация и кристаллизация до тех пор, пока не будет получена неорганическая соль. В этом соединении олово потеряло два электрона из его валентной оболочки, чтобы сформировать связи с атомами хлора.
Это может быть лучше понято, если учесть валентную конфигурацию олова (5 с25pх2ри0рZ0), из которых пара электронов занимает орбиталь рх дается протонам H+, для того, чтобы сформировать двухатомную молекулу водорода. То есть это реакция окислительно-восстановительного типа.
индекс
- 1 Физико-химические свойства
- 1.1 Конфигурация Валенсии
- 1.2 Реакционная способность
- 1.3 Восстановительная активность
- 2 Химическая структура
- 3 использования
- 4 риска
- 5 ссылок
Физико-химические свойства
Ссылки SnCl2 Они ионные или ковалентные? Физические свойства хлорида олова (II) исключают первый вариант. Точки плавления и кипения для этого соединения составляют 247 ° C и 623 ° C, что свидетельствует о слабых межмолекулярных взаимодействиях, что является распространенным фактом для ковалентных соединений..
Его кристаллы белого цвета, что приводит к нулевому поглощению в видимом спектре.
Конфигурация Валенсии
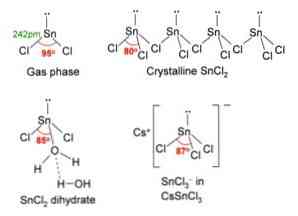
На изображении выше, в верхнем левом углу, показана изолированная молекула SnCl2.
Молекулярная геометрия должна быть плоской, потому что гибридизация центрального атома является sp2 (3 орбитальных зр2 и чистой орбитали для образования ковалентных связей), но свободная пара электронов занимает объем и отталкивает атомы хлора вниз, придавая молекуле угловую геометрию.
В газовой фазе это соединение изолировано, поэтому оно не взаимодействует с другими молекулами.
Как потеря пары электронов на орбите рх, олово превращается в ион Sn2+ и его итоговая электронная конфигурация составляет 5 с25pх0ри0рZ0, со всеми его p-орбиталями, доступными для приема ссылок от других видов.
Ионы Cl- координировать с ионом Sn2+ дать хлорид олова. Электронная конфигурация олова в этой соли составляет 5 с25pх2ри2рZ0, возможность принять другую пару электронов в своей свободной орбитальной рZ.
Например, вы можете принять другой ион Cl-, образующий комплекс геометрии треугольной плоскости (пирамида с треугольным основанием) и отрицательно заряженный [SnCl3]-.
реактивность
SnCl2 имеет высокую реакционную способность и склонность вести себя как кислота Льюиса (электронный рецептор), чтобы завершить свой валентный октет.
Так же, как он принимает ион Cl-, то же самое происходит с водой, которая «гидратирует» атом олова, связывая молекулу воды непосредственно с оловом, и вторая молекула воды образует взаимодействия водородных связей с первым.
Результатом этого является то, что SnCl2 это не чисто, но согласовано с водой в его дигидратированной соли: SnCl2· 2Н2О.
SnCl2 Он очень растворим в воде и в полярных растворителях, потому что это полярное соединение. Однако его растворимость в воде, меньшая, чем его массовый вес, активирует реакцию гидролиза (разрыв молекулы воды) с образованием основной и нерастворимой соли:
SnCl2(вод) + H2O (l) <=> Sn (OH) Cl (s) + HCl (водн.)
Двойная стрелка указывает на то, что установлено равновесие, благоприятное для левой стороны (по отношению к реагентам), если концентрации HCl увеличиваются. Для этого растворы SnCl2 используемый имеет кислотный рН, чтобы избежать осаждения нежелательного солевого продукта гидролиза.
Восстановительная активность
Реагирует с кислородом в воздухе с образованием хлорида олова (IV) или хлорида олова:
6 SnCl2(aq) + O2(г) + 2Н2O (l) => 2SnCl4(aq) + 4Sn (OH) Cl (s)
В этой реакции олово окисляется, образуя связь с электроотрицательным атомом кислорода и увеличивает количество связей с атомами хлора..
В целом, электроотрицательные атомы галогенов (F, Cl, Br и I) стабилизируют связи соединений Sn (IV), и этот факт объясняет, почему SnCl2 это восстановитель.
Когда он окисляется и теряет все свои валентные электроны, ион Sn4+ это остается с конфигурацией 5s05pх0ри0рZ0, будучи парой электронов в орбитальных 5-ых, наиболее трудно быть «схваченным».
Химическая структура
SnCl2 представлена кристаллическая структура орторомбического типа, похожая на ряды пил, в которых кончики зубов представляют собой хлориды.
Каждый ряд представляет собой цепь SnCl3 образуя мостик Cl с другим атомом Sn (Cl-Sn (Cl)2-Cl- ···), как видно на изображении выше. Две цепи, связанные слабыми взаимодействиями типа Sn-Cl, составляют один слой расположения, который накладывается на другой слой и так далее, пока не будет определено кристаллическое твердое вещество..
Свободная электронная пара 5s2 вызывает искажения в структуре, потому что он занимает объем (объем электронного облака).
Sn может иметь координационное число, равное девяти, то же самое, что иметь девять соседей, рисуя тригональную призму с этим, расположенным в центре геометрической фигуры, и Cl в вершинах, в дополнение к другим Cl, расположенным в каждом квадратных граней призмы.
Это легче заметить, если рассмотреть цепь, в которой Sn (темно-серые сферы) направлены вверх, а три Cl, связанные с ней, образуют треугольный пол, а три верхних Cls образуют треугольную крышу..
приложений
В органическом синтезе он используется в качестве восстановителя для ароматических нитросоединений (Ar-NO2 à Ar-NH2). Поскольку его химическая структура является ламинарной, он находит применение в мире катализа органических реакций, помимо того, что является потенциальным кандидатом на каталитическую поддержку.
Его восстановительное свойство используется для определения присутствия соединений золота, для покрытия стекол серебряными зеркалами и для действия в качестве антиоксиданта..
Также в своей молекулярной геометрии тригональная пирамида (: SnX3- M+) используется в качестве основы Льюиса для синтеза большого количества соединений (таких как кластерный комплекс Pt)3Sn8Cl20, где безэлектронная пара координируется с кислотой Льюиса).
риски
SnCl2 Это может повредить лейкоциты. Он вызывает коррозию, раздражение, канцерогенность и оказывает сильное негативное воздействие на виды, обитающие в морских экосистемах..
Он может разлагаться при высоких температурах, выделяя вредный газообразный хлор. При контакте с высокоокислительными агентами вызывает взрывные реакции.
ссылки
- Дрожь и Аткинс. (2008). Неорганическая химия в Элементы группы 14 (четвертое издание., стр. 329). Mc Graw Hill.
- ChemicalBook. (2017). Получено 21 марта 2018 года из ChemicalBook: chemicalbook.com
- PubChem. (2018). Хлорид олова. Получено 21 марта 2018 года из PubChem: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2017). Хлорид олова (II). Получено 21 марта 2018 года из Википедии: en.wikipedia.org
- Э. Г. Рохов, Э. У. (1975). Химия германия: олово и свинец (первое издание). п-82.83. Pergamom Press.
- Ф. Хулигер. (1976). Структурная химия фаз слоистого типа. P-120121. Издательство Д. Рейдел.



