Йодоат калия свойства, структура, использование и риски
йодат калия или йодат калия представляет собой неорганическое соединение йода, в частности соль, химическая формула которой KIO3. Йод, элемент группы галогенов (F, Cl, Br, I, As), имеет в этой соли степень окисления +5; из-за этого это сильный окислитель. КИО3 диссоциирует в водной среде, чтобы создать ионы К+ и IO3-.
Он синтезируется путем взаимодействия гидроксида калия с йодной кислотой: HIO3(aq) + KOH (s) => KIO3(вод) + H2O (l) Кроме того, он может быть синтезирован путем взаимодействия молекулярного йода с гидроксидом калия: 3I2(s) + 6KOH (s) => KIO3(aq) + 5KI (aq) + 3H2O (l).

индекс
- 1 Физико-химические свойства
- 1.1 Окисляющий агент
- 2 Химическая структура
- 3 Применение и применение йодата калия
- 3.1 Терапевтическое использование
- 3.2 Использование в промышленности
- 3.3 Аналитическое использование
- 3.4 Использование в технологии лазеров
- 4 Риски для здоровья йодата калия
- 5 ссылок
Физико-химические свойства
Это белое твердое вещество без запаха, с мелкими кристаллами и кристаллической структурой моноклинного типа. Он имеет плотность 3,98 г / мл, молекулярную массу 214 г / моль и имеет полосы поглощения в инфракрасном (ИК) спектре..
Он имеет температуру плавления: 833 ºK (560 ºC), что соответствует сильным ионным взаимодействиям между ионами K+ и IO3-. При более высоких температурах он подвергается реакции термического разложения с выделением молекулярного кислорода и йодида калия:
2KIO3(s) => 2KI (s) + 302(G)
Растворимость в воде варьируется от 4,74 г / 100 мл до 0ºC, до 32,3 г / 100 мл при 100ºC, образуя бесцветные водные растворы. Кроме того, он нерастворим в спирте и азотной кислоте, но растворим в разбавленной серной кислоте.
Его сродство к воде не заметно, что объясняет, почему он не гигроскопичен и не существует в форме гидратированных солей (KIO)3· H2O).
Окисляющий агент
Йодат калия, как указано в его химической формуле, содержит три атома кислорода. Это сильно электроотрицательный элемент, и благодаря этому свойству он «обнаруживает» электронный дефицит в облаке, окружающем йод.
Этот недостаток или вклад, в зависимости от обстоятельств, можно рассчитать как степень окисления йода (± 1, +2, +3, +5, +7), равную +5 для случая этой соли.
Что это значит? Что перед видом, способным давать свои электроны, йод примет их в их ионной форме (IO3-) стать молекулярным йодом и иметь степень окисления, равную 0.
Следуя этому объяснению, можно определить, что йодат калия является окислительным соединением, которое сильно реагирует с восстановителями во многих окислительно-восстановительных реакциях; один из них известен как йодные часы.
Йодные часы состоят из окислительно-восстановительного процесса медленных и быстрых шагов, в которых быстрые шаги отмечены решением KIO3 в серной кислоте, к которой добавлен крахмал. Далее, крахмал - когда-то произведенный и закрепленный между его структурой I видов3-- превратит раствор из бесцветного в темно-синий.
IO3- + 3 HSO3- → я- + 3 HSO4-
IO3- + 5 я- + 6 ч+ → 3 я2 + 3 ч2О
Я2 + HSO3- + H2O → 2 I- + HSO4- + 2 ч+ (темно-синий из-за эффекта крахмала)
Химическая структура
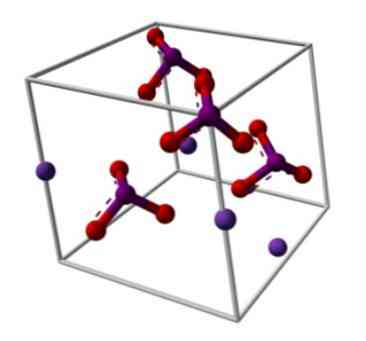
Химическая структура йодата калия показана на верхнем изображении. Анион IO3- представлен «штатив» из красных и пурпурных сфер, а ионы К+ они представлены фиолетовыми сферами.
Но что означают эти штативы? Правильные геометрические формы этих анионов на самом деле представляют собой тригональные пирамиды, в которых атомы кислорода образуют треугольное основание, а неразделенная пара электронов в йоде указывает вверх, занимая пространство и заставляя IO-связь вниз, а две ссылки I = O.
Эта молекулярная геометрия соответствует sp-гибридизации3 центрального атома йода; однако другая точка зрения предполагает, что один из атомов кислорода образует связи с «d» -орбиталами йода, фактически являясь sp-гибридизацией3d2 (у йода могут быть "d" орбитали, расширяющие его валентную оболочку).
Кристаллы этой соли могут претерпевать переходы структурной фазы (другие структуры, кроме моноклинной) вследствие различных физических условий, которые их подвергают..
Использование и применение йодата калия
Терапевтическое использование
Йодат калия обычно используется для предотвращения накопления радиоактивности в щитовидной железе в виде 131I, когда этот изотоп используется при определении поглощения йода щитовидной железой как компонента функционирования щитовидной железы.
Кроме того, йодат калия используется в качестве местного антисептика (0,5%) при инфекциях слизистой оболочки.
Использование в промышленности
Добавляется в корм сельскохозяйственных животных в качестве йодной добавки. Поэтому в промышленности йодат калия используется для улучшения качества муки.
Аналитическое использование
В аналитической химии благодаря своей стабильности он используется в качестве основного стандарта при стандартизации стандартных растворов тиосульфата натрия (Na2S2О3), чтобы определить концентрации йода в образцах.
Это означает, что количество йода может быть известно с помощью объемных методов (титрования). В этой реакции йодат калия быстро окисляет йодид-ионы I-, по следующему химическому уравнению:
IO3- + 5I- + 6H+ => 3I2 + 3H2О
Йод, я2, называется с раствором Na2S2О3 для его стандартизации.
Использование в технологии лазеров
Исследования продемонстрировали и подтвердили интересные пьезоэлектрические, пироэлектрические, электрооптические, сегнетоэлектрические свойства и нелинейную оптику кристаллов KIO.3. Это приводит к огромному потенциалу в области электроники и технологии лазеров для материалов, изготовленных из этого соединения..
Риски для здоровья йодата калия
В больших дозах может вызывать раздражение слизистой оболочки полости рта, кожи, глаз и дыхательных путей.
Эксперименты по токсичности йодата калия у животных позволили заметить, что у собак, соблюдающих голодание, в дозах 0,2-0,25 г / кг массы тела, вводимых перорально, соединение вызывает рвоту.
Если избежать этих рвот, это вызывает ухудшение ситуации у животных, так как вызывает смерть от анорексии и прострации. Его вскрытия позволили наблюдать некротические поражения печени, почек и слизистой оболочки кишечника..
Из-за своей окислительной способности он представляет риск возгорания при контакте с легковоспламеняющимися материалами..
ссылки
- Дей Р. и Андервуд А. Количественная аналитическая химия (пятое изд.). Пирсон Прентис Холл, р-364.
- Мут, Д. (2008). Лазеры. [Рисунок]. Получено с: flickr.com
- ChemicalBook. (2017). Калия йодат. Получено 25 марта 2018 года с сайта ChemicalBook: chemicalbook.com
- PubChem. (2018). Йодат калия. Получено 25 марта 2018 года из PubChem: pubchem.ncbi.nlm.nih.gov
- Merck. (2018). Калий йодат. Получено 25 марта 2018 года из Мерк:
- merckmillipore.com
- Wikipedia. (2017). Калий йодат. Получено 25 марта 2018 года из Википедии: en.wikipedia.org
- М. М. Абдель Кадер и соавт. (2013). Механизм переноса заряда и низкотемпературные фазовые переходы в КИО3. J. Phys.: Conf. Ser. 423 012036


