Структура оксида серебра (Ag2O), свойства, номенклатура и применение
оксид серебра неорганическое соединение, чья химическая формула Ag2О. Сила, которая объединяет его атомы, имеет полностью ионную природу; следовательно, он состоит из ионного твердого тела, в котором существует соотношение двух катионов Ag+ электростатически взаимодействуя с анионом О2-.
Оксид-анион, О2-, это происходит в результате взаимодействия атомов серебра на поверхности с кислородом окружающей среды; очень похоже на железо и многие другие металлы. Серебряное изделие или украшение вместо того, чтобы краснеть и рассыпаться в ржавчину, становится черным, характерным для оксида серебра.

Например, на изображении выше вы можете увидеть ржавую серебряную чашку. Обратите внимание на его почерневшую поверхность, хотя он все еще сохраняет некоторый декоративный блеск; поэтому даже ржавые серебряные предметы можно считать достаточно привлекательными для декоративного использования.
Свойства оксида серебра таковы, что они не портят, на первый взгляд, первоначальную металлическую поверхность. Это сформировано при комнатной температуре простым контактом с кислородом в воздухе; и что еще интереснее, он может разлагаться при высоких температурах (выше 200 ° C).
Это означает, что если удерживать стекло изображения и применять тепло интенсивного пламени, оно восстановит свой серебристый блеск. Следовательно, его образование является термодинамически обратимым процессом..
Оксид серебра также имеет другие свойства и, помимо своей простой формулы Ag2Или это охватывает сложные структурные организации и богатое разнообразие твердых веществ. Тем не менее, Ag2Или это возможно, рядом с Ag2О3, самый представительный из оксидов серебра.
индекс
- 1 Структура оксида серебра
- 1.1 Изменения в количестве Валенсии
- 2 Физические и химические свойства
- 2.1 Молекулярный вес
- 2.2 Внешний вид
- 2.3 Плотность
- 2.4 Точка плавления
- 2,5 кпс
- 2.6 Растворимость
- 2.7 Ковалентный характер
- 2.8 Разложение
- 3 Номенклатура
- 3.1 Валенсия I и III
- 3.2 Систематическая номенклатура сложных оксидов серебра
- 4 использования
- 5 ссылок
Структура оксида серебра
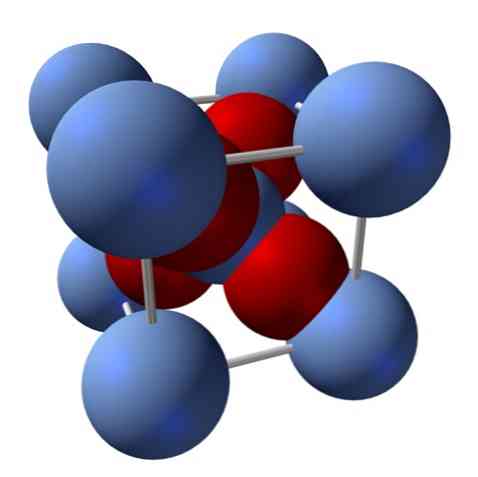
Как его структура? Как уже упоминалось в начале: это ионное тело. По этой причине в его структуре не может быть ковалентных связей Ag - O и Ag = O; поскольку, если бы они были, свойства этого оксида резко изменились бы. Именно тогда ионы Ag+ и O2- в соотношении 2: 1 и испытывает электростатическое притяжение.
Структура оксида серебра определяется, следовательно, тем, как ионные силы распределяют в пространстве ионы Ag.+ и O2-.
Например, на верхнем изображении у вас есть элементарная ячейка для кубической кристаллической системы: катионы Ag+ серебристо-синие сферы, а O2- красноватые сферы.
Если вы посчитаете количество сфер, вы обнаружите, что на первый взгляд есть девять серебристо-голубых и четыре красных цвета. Однако принимаются во внимание только фрагменты сфер, содержащихся в кубе; считая их, как доли от общего количества сфер, нужно соблюдать соотношение 2: 1 для Ag2О.
Повторяя структурную единицу тетраэдра AgO4 в окружении четырех других Ag+, все черное тело построено (устранение пробелов или неровностей, которые могут иметь эти кристаллические структуры).
Изменения в количестве Валенсии
Сосредоточение теперь не на тетраэдре AgO4 но в линии AgOAg (обратите внимание на вершины верхнего куба) будет показано, что твердое вещество оксида серебра состоит, с другой точки зрения, из множества ионных слоев, расположенных линейно (хотя и наклонно). Все это в результате «молекулярной» геометрии вокруг Ag+.
Вышесказанное было подтверждено несколькими исследованиями его ионной структуры.
Серебро работает преимущественно с валентностью +1, поскольку при потере электрона его электронная конфигурация равна [Kr] 4d.10, который очень стабилен. Другие валентности, такие как Ag2+ и Ag3+ они менее стабильны, так как теряют электроны от орбиталей, почти полностью заполненных.
Ag ион3+, однако он относительно менее нестабилен по сравнению с Ag2+. На самом деле, он может сосуществовать в компании Ag+ Химически обогащает структуру.
Его электронная конфигурация [Kr] 4d8, с неспаренными электронами таким образом, что дает ему некоторую стабильность.
В отличие от линейной геометрии вокруг ионов Ag+, было обнаружено, что это из ионов Ag3+ Это квадратная квартира. Следовательно, оксид серебра с ионами Ag3+ будет состоять из слоев, состоящих из квадратов AgO4 (не тетраэдры), электростатически связанные линиями AgOAg; Таков случай Ag4О4 или Ag2O ∙ Ag2О3 с моноклинной структурой.
Физико-химические свойства

Если вы поцарапаете поверхность серебряного стакана основного изображения, вы получите твердое тело, которое не только черного цвета, но также имеет коричневые или коричневые тона (верхнее изображение). Некоторые из его физических и химических свойств, о которых сообщают моменты, следующие:
Молекулярный вес
231 735 г / моль
внешний вид
Твердый черный коричневый в виде порошка (обратите внимание, что, несмотря на то, что он является ионным твердым веществом, он не имеет кристаллического вида). Он не имеет запаха и смешан с водой, придает ему металлический привкус
плотность
7,14 г / мл.
Точка плавления
277-300 ° С Конечно, он плавится в твердое серебро; то есть он, вероятно, разрушается до образования жидкого оксида.
КПС
1,52 ∙ 10-8 в воде при 20 ° С Поэтому это соединение плохо растворимое в воде.
растворимость
Если вы внимательно посмотрите на изображение его структуры, вы обнаружите, что сферы Ag2+ и O2- Они не расходятся почти по размеру. В результате только небольшие молекулы могут проникать внутрь кристаллической решетки, делая ее нерастворимой почти во всех растворителях; за исключением тех, где он реагирует, таких как основания и кислоты.
Ковалентный персонаж
Хотя неоднократно говорилось, что оксид серебра является ионным соединением, некоторые свойства, такие как его низкая температура плавления, противоречат этому утверждению..
Конечно, рассмотрение ковалентного характера не нарушает того, что объясняется для его структуры, было бы достаточно, чтобы добавить его к структуре Ag2Или модель сфер и стержней для обозначения ковалентных связей.
Также тетраэдры и квадратные плоскости AgO4, как и линии AgOAg, они будут связаны ковалентными (или ковалентными ионными) связями.
Имея это в виду, Ag2Или это на самом деле полимер. Тем не менее, рекомендуется рассматривать его как ионное твердое вещество с ковалентным характером (характер связи до сих пор остается проблемой).
разложение
Сначала было упомянуто, что его образование является термодинамически обратимым, поэтому он поглощает тепло, чтобы вернуться в свое металлическое состояние. Все это можно выразить двумя химическими уравнениями для таких реакций:
4Ag (s) + O2(г) => 2Ag2O (s) + Q
2AG2O (s) + Q => 4Ag (s) + O2(G)
Где Q представляет тепло в уравнении. Это объясняет, почему огонь, сжигающий поверхность ржавой серебряной чашки, возвращает свой серебристый блеск.
Поэтому трудно предположить, что существует Ag2O (l), так как оно мгновенно разлагается под воздействием тепла; если только давление не является слишком высоким для получения указанной коричневой черной жидкости.
номенклатура
Когда появилась возможность введения ионов Ag2+ и Ag3+ помимо общего и преобладающего Ag+, термин «оксид серебра» начинает казаться недостаточным для обозначения Ag2О.
Это потому, что ион Ag+ является более распространенным, чем другие, поэтому Аг2Или как единственный оксид; что совсем не правильно.
Если вы считаете, Ag2+ так как практически не существует, учитывая его нестабильность, то будут присутствовать только ионы с валентностями +1 и +3; то есть Ag (I) и Ag (III).
Валенсия I и III
Поскольку Ag (I) является наименее валентным, его называют путем добавления суффикса -oso к его имени. Argentum. Итак, Аг2Или это: окись аргентозо или, согласно систематической номенклатуре, окись диплата.
Если Ag (III) полностью игнорируется, то его традиционная номенклатура должна быть: оксид серебра вместо оксида аргентина.
С другой стороны, Ag (III), являющийся большей валентностью, добавляет к своему имени суффикс -ico. Итак, Аг2О3 это: оксид серебра (2 Ag ионы)3+ с тремя O2-). Кроме того, его название в соответствии с систематической номенклатурой будет: диплат триоксид.
Если структура Ag наблюдается2О3, можно предположить, что это продукт окисления озоном, ИЛИ3, вместо кислорода. Следовательно, его ковалентный характер должен быть больше, поскольку он представляет собой ковалентное соединение со связями Ag-O-O-O-Ag или Ag-O.3-Ag.
Систематическая номенклатура сложных оксидов серебра
AgO, также написано как Ag4О4 или Ag2O ∙ Ag2О3, это оксид серебра (I, III), так как он имеет обе валентности +1 и +3. Его название в соответствии с систематической номенклатурой будет: тетраплат тетраоксид.
Эта номенклатура очень помогает, когда речь идет о других стехиометрически более сложных оксидах серебра. Например, предположим, что два твердых вещества 2Ag2O ∙ Ag2О3 и Ag2O ∙ 3Ag2О3.
Написание первого более подходящим способом будет следующим: Ag6О5 (считая и добавляя атомы Ag и O). Его имя тогда будет гексаплатной пятиокисью. Обратите внимание, что этот оксид имеет состав серебра менее богатый, чем Ag2О (6: 5 < 2:1).
При написании второго твердого тела в противном случае это будет: Ag8О10. Его название будет декапоксид октаплата (с соотношением 8:10 или 4: 5). Этот гипотетический оксид серебра будет "очень окисленным".
приложений
Исследования в поисках новых и сложных применений для оксида серебра все еще проводятся сегодня. Некоторые из его использования перечислены ниже:
-Он растворяется в аммиаке, аммиачной селитре и воде с образованием реагента Tollens. Этот реагент является полезным инструментом для качественного анализа в лабораториях органической химии. Это позволяет определить наличие альдегидов в образце, положительным ответом которого является образование «серебряного зеркала» в пробирке..
-Вместе с металлическим цинком он образует первичные батареи из оксида цинка серебра. Это, пожалуй, одно из самых распространенных и домашних применений.
-Он служит в качестве очистителя газа, поглощая, например, СО2. При нагревании выделяет захваченные газы и может быть повторно использован несколько раз..
-Благодаря антимикробным свойствам серебра, его оксид полезен в исследованиях биоанализа и очистки почвы..
-Это мягкий окислитель, способный окислять альдегиды до карбоновых кислот. Он также используется в реакции Гофмана (третичные амины) и участвует в других органических реакциях, в качестве реагента или катализатора..
ссылки
- Бергстрессер М. (2018). Оксид серебра: формула, разложение и образование. Исследование. Получено с: study.com
- Авторы и редакторы томов III / 17E-17F-41C. (Н.Д.). Кристаллическая структура оксидов серебра (Ag (x) O (y)), параметры решетки. (Числовые данные и функциональные связи в науке и технике), том 41C. Спрингер, Берлин, Гейдельберг.
- Махендра Кумар Триведи, Рама Мохан Таллапрагада, Алиса Брантон, Дахрин Триведи, Гопал Наяк, Омпракаш Латиял, Снехасис Яна. (2015). Потенциальное влияние энергетической обработки биополя на физические и термические свойства порошка оксида серебра. Международный журнал биомедицинской науки и техники. Том 3, № 5, с. 62-68. doi: 10.11648 / j.ijbse.20150305.11
- Салливан Р. (2012). Разложение оксида серебра. Университет Орегона Получено от: chemdemos.uoregon.edu
- Флинт, Деянда. (24 апреля 2014 г.) Использование серебряных оксидных батарей. Sciencing. Получено от: sciencing.com
- Салман Монтасир Э. (2016). Исследование некоторых оптических свойств оксида серебра (Ag2o) с помощью спектрофотометра UVVisible. [PDF]. Получено с: iosrjournals.org
- Бард Аллен Дж. (1985). Стандартные потенциалы в водном растворе. Марсель Деккер. Получено с: books.google.co.ve


