Реакция омыления и вещества, которые можно получить
омыление Это основной гидролиз сложного эфира. Это означает, что сложный эфир необратимо реагирует с основанием (NaOH или KOH), образуя спирт и карбоксилаты натрия или калия. Слово означает «производство мыла» и, по сути, является одной из древнейших химических реакций, используемых человечеством..
В вавилонские времена с помощью золы, собранной из дерева, растений и животных жиров, они усовершенствовали искусство изготовления мыла. Почему животный жир? Причина в том, что он богат глицериновыми триэфирами (триглицеридами), а древесная зола является источником калия, основного металла.
В противном случае реакция протекает с меньшим выходом, но этого достаточно, чтобы отразить его воздействие на краски и некоторые поверхности. Так обстоит дело с картинами маслом, где пигменты смешиваются с маслом (источник сложных эфиров).
индекс
- 1 реакция омыления
- 1.1 Механизм
- 1.2 Кинетика
- 2 Вещества, которые можно получить омылением
- 2.1 Растворительное действие мыла
- 3 Ссылки
Реакция омыления
механизм
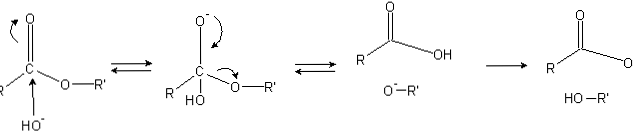
Сложные эфиры имеют ацильную группу (O = C-R), которая подвержена нуклеофильным атакам, таким как ОН-.
Поскольку атомы кислорода «крадут» электронную плотность у атома углерода, он частично заряжен, особенно в случае сложных эфиров..
Следовательно, этот положительный заряд привлекает отрицательные частицы, способные доставлять электроны к атому углерода, при этом происходит нуклеофильная атака (левая сторона изображения). В результате образуется тетраэдрический интермедиат (вторая молекула слева направо).
Отрицательный заряд на кислороде тетраэдрического интермедиата является продуктом ОН- окружающих. Затем этот отрицательный заряд делокализуется, образуя карбонильную группу, «заставляя» затем разорвать связь C-OR '. Кроме того, это перемещение производит карбоновую кислоту RCOOH и алкоксидный ион R'O-.
Наконец, поскольку реакционная среда является основной, алкоксид депротонирует одну молекулу воды, а карбоновая кислота реагирует с другим ОН- среды, генерирующей продукты омыления.
кинетика
Скорость реакции омыления пропорциональна концентрации реагентов. Другими словами, увеличивая концентрацию сложного эфира (RCOOR ') или основания (NaOH), реакция будет протекать с более высокой скоростью..
Это также переводится следующим образом: скорость омыления первого порядка по отношению к эфиру и первого порядка по основанию. Сказанное можно выразить следующим математическим уравнением:
Скорость = k [RCOOR '] [NaOH]
Где k - коэффициент постоянной или скорости, который изменяется как функция температуры или давления; то есть, чем выше температура, тем выше скорость омыления. По этой причине среда подвергается кипению.
Поскольку оба реагента являются кинетическими первого порядка, общая реакция составляет второй порядок.
В механизме реакции омыления образование тетраэдрического интермедиата требует нуклеофильной атаки, которая включает как сложный эфир, так и основание..
Таким образом, кинетика второго порядка отражается в этом факте, потому что они вмешиваются в (медленную) детерминантную стадию реакции.
Вещества, которые можно получить омылением

Основными продуктами омыления являются спирты и соли карбоновых кислот. В кислой среде получают соответствующий RCOOH, полученный омылением жиров и масел, которые известны как жирные кислоты..
Таким образом, мыла состоят из солей жирных кислот, образующихся в результате омыления. Вы выходите с какими катионами? Они могут быть на+, К+, мг2+, вера3+, и т.д..
Эти соли растворимы в воде, но осаждаются под действием NaCl, добавляемого в смесь, которая обезвоживает мыло и отделяет его от водной фазы. Реакция омыления для триглицерида является следующей:
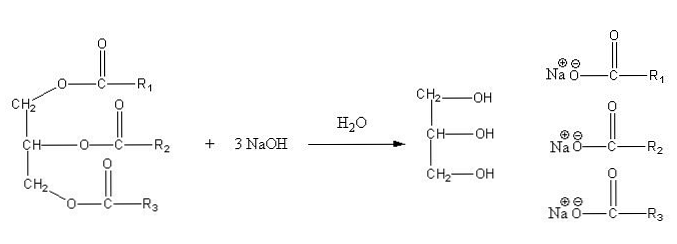
Глицерин - это алкогольное «Е», а мыло - это все соли образующихся жирных кислот. Здесь каждая боковая цепь -R имеет разную длину и степень ненасыщенности. Следовательно, эти цепи делают разницу между жирами и растительными маслами.
В этом случае ключ к производству мыла лежит в выборе лучших жиров и масел или, более конкретно, в выборе различных источников триглицеридов..
Эта белая мыльная масса может содержать в своей структуре красители и другие органические соединения, придавая ей приятные ароматы и яркие цвета. Отсюда, диапазон возможностей приручен искусством и призванием в этой торговле.
Однако реакция омыления также является синтетическим путем карбоновых кислот и спиртов, которые необязательно связаны с глицерином или мылом..
Например, основной гидролиз любого эфира, такого как простой этилацетат, приведет к получению уксусной кислоты и этанола.
Растворительное действие мыла

Соли жирных кислот растворимы в воде, но не так, как сольваты ионов; то есть в окружении водной сферы. В случае мыла их боковые цепи -R предотвращают их теоретическое растворение в воде.
Поэтому, чтобы противодействовать этой энергетически неудобной позиции, они ориентированы таким образом, что эти цепи вступают в контакт, образуя неполярное органическое ядро, а полярные головки - конец (-COO)- не доступно+), взаимодействовать с молекулами воды и создавать «полярную оболочку».
Выше показано на изображении выше, где показан этот тип структуры, известный как мицелла.
«Черные хвосты» соответствуют гидрофобным цепям, запутываясь в органическом ядре, защищенном серыми сферами. Эти серые сферы составляют полярный щит, головы -COO- не доступно+.
Затем мицеллы представляют собой скопления (скопления) солей жирных кислот. В них они могут содержать жир, который нерастворим в воде из-за его неполярного характера.
Как они это делают? И жир, и цепи -R являются гидрофобными, поэтому оба имеют большое сродство друг к другу.
Когда мицеллы окружают жиры, вода взаимодействует с полярной оболочкой, обеспечивая растворимость мыла. Аналогично, мицеллы заряжены отрицательно, вызывая отталкивание друг к другу и, следовательно, вызывая дисперсию жира.
ссылки
- Энн Мари Хельменстин, доктор философии (3 октября 2017 г.) Определение омыления и реакция. Получено 24 апреля 2018 г.
- Фрэнсис А. Кэри. Органическая химия Карбоновые кислоты. (шестое издание., стр. 863-866). Mc Graw Hill.
- Грэм Соломонс Т.В., Крейг Б. Фрайл. Органическая химия. Липиды (10-е издание., Стр. 1056-1058). Wiley Plus.
- Wikipedia. (2018). Омыления. Получено 24 апреля 2018 г. с сайта en.wikipedia.org
- Бойд С. (27 февраля 2015 г.). Понять химию и историю мыла. Получено 24 апреля 2018 г. по адресу: chemservice.com
- Лука Лаги (27 марта 2007 г.) Омыления. Получено 24 апреля 2018 г. с сайта commons.wikimedia.org.
- Аманда Кроше (12 мая 2015 г.) Мицель (оттенки серого). Получено 24 апреля 2018 г. с сайта commons.wikimedia.org.


