Химическая структура, свойства и применение пропилена
пропилен или пропен при комнатной температуре и при атмосферном давлении находится в газообразном состоянии и, как и другие алкены, бесцветен. Он имеет запах, похожий на масло, но менее интенсивный. Он имеет дипольный момент, поскольку, хотя ему не хватает сильной полярной связи, его молекула асимметрична.
Также пропилен является структурным изомером циклопропана (они имеют одинаковую химическую формулу C)3H6). Это происходит в природе как следствие процессов вегетации и брожения. Искусственно встречается при переработке ископаемых видов топлива, таких как нефть, природный газ и, в меньшей степени, углерод.

Аналогичным образом, этилен и пропилен являются продуктами переработки нефти в процессе расщепления больших углеводородных молекул с образованием небольших углеводородов, пользующихся высоким спросом..
Пропилен также может быть получен с использованием различных методологий:
- Реагирует обратимо на этилен и бутен, где двойные связи разрываются и переформулируются для получения пропилена.
- Через процесс дегидрирования (потери водорода) пропана.
- В рамках программы по производству олефинов из метанола (МТО), пропилен был произведен из метанола. Это было пропущено через цеолитный катализатор, который способствует его дегидратации и приводит к образованию этилена и пропилена..
3CH3ОН (метанол) => СН3CH = CH2 (пропилен) + 3Н2O (вода)
индекс
- 1 Химическая структура
- 2 свойства
- 2.1 Молекулярный вес
- 2.2 Точка кипения
- 2.3 Точка плавления
- 2.4 Температура вспышки
- 2.5 Растворимость
- 2.6 Растворимость, выраженная как масса
- 2.7 Плотность
- 2.8 Плотность пара
- 2.9 Давление пара
- 2.10 Самовоспламенение
- 2.11 Вязкость
- 2.12 Теплота сгорания
- 2.13 Тепло испарения
- 2.14 Поверхностное натяжение
- 2.15 Полимеризация
- 2.16 Точка замерзания
- 2.17 Порог запаха
- 3 использования
- 3.1 Полипропилен
- 3.2 Акрилонитрил
- 3.3 Пропиленоксид
- 3.4 Для синтеза спиртов и других целей
- 4 Ссылки
Химическая структура
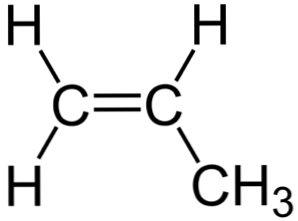
На изображении выше видна химическая структура пропилена, в которой выделяется его асимметрия (правая сторона отличается от левой). Его углеродный скелет, не считая атомов H, можно наблюдать как бумеранг.
Этот бумеранг представляет ненасыщенность или двойную связь на одной из его сторон (C1) и, следовательно, он плоский из-за sp-гибридизации2 атомов углерода.
Однако другая сторона занята метильной группой (-CH3), чья гибридизация является sp3 и он имеет тетраэдрическую геометрию. Таким образом, если смотреть спереди, бумеранг плоский с атомами H, выступающими из этого на 109,5º приблизительно.
В газовой фазе молекула слабо взаимодействует с другими силами дисперсии. Кроме того, метильная группа предотвращает взаимодействие между двойными связями (π-π) двух молекул пропилена..
Это приводит к уменьшению их межмолекулярных сил, что отражается на их физических свойствах. Только при очень низких температурах пропилен может принять твердую структуру, в которой бумеран остается сгруппированным со своими слабыми взаимодействиями.
свойства
Это бесцветный газ с ароматическим запахом. Он транспортируется в виде сжиженного газа и, когда он выходит из контейнеров, в которых он находится, он делает это в форме газа или жидкости. При низких концентрациях он образует взрывоопасную и легковоспламеняющуюся смесь с воздухом, плотность пропилена выше, чем у воздуха.
Молекулярный вес
42 081 г / моль
Точка кипения
От 53,9 ºF до 760 мм рт.ст.
От 48 ºC до 760 мм рт.ст.
Точка плавления
301,4 ºF
185 ºC
Точка вспышки
162 ºF
растворимость
44,6 мл / 100 мл в воде.
1250 мл / 100 мл в этаноле.
524,5 мл / 100 мл в уксусной кислоте.
Растворимость, выраженная как масса
200 мг / л 25 ºC
плотность
0,609 мг / мл при -52,6º F
0,5139 при 20º C
Плотность пара
От 1,46 до 32 ° F (относительно воздуха, взятого для сравнения).
1,49 (воздух = 1).
1,91 кг / м3 до 273,15 ºK
Давление пара
1 мм рт.ст. при -205,4ºF
760 мм рт.ст. до -53,9 ° F
8,69 × 103 мм рт.ст. при 25 ºC (экстраполированное значение).
1158 кПа при 25 ºC
15,4 атм при 37 ºC
самовоспламенение
851 ºF
455 ºC
вязкость
83,4 микропузы при 16,7 ° С.
Теплота сгорания
16 692 БТЕ / фунт
10,940 кал / г
Тепло испарения
104,62 кал / г (при температуре кипения)
Поверхностное натяжение
16,7 дин / см при 90 ° С
полимеризация
Полимеризуется при высоких температурах и высоких давлениях в присутствии катализаторов.
Точка замерзания
185,25 ° C.
Порог запаха
10-50 мг / м3 (Обнаружение)
100 мг / м3 (Признание)
приложений

Используется в нефтехимической промышленности в качестве топлива и алкилирующего агента. В химической промышленности его используют в качестве сырья для производства и синтеза многочисленных производных..
Он полезен в основном для производства полипропилена, акрилонитрила (ACN), пропиленоксида (PO), спиртов, кумола и акриловых кислот..
полипропилен
Полипропилен является одним из основных пластиковых материалов, используемых в электронике и электротехнике, предметах домашнего обихода, крышках от бутылок и чемоданах..
Ламинированный материал используется для упаковки конфет, этикеток, компакт-дисков и т. Д., А волокна - из папок и одежды..
акрилонитрил
Эластомерные полимеры и волокна получают из акрилонитрила. Эти волокна предназначены для изготовления разных форм одежды, таких как кофты, носки и спортивная одежда. Они также используются в домашней мебели, в папках, обивке, подушках и одеялах.
Окись пропилена
Оксид пропилена участвует в качестве компонента в синтезе полиуретана. Это используется в производстве гибкой пены и жесткой пены. Гибкая пена используется в качестве наполнителя для домашней мебели и в автомобильной промышленности..
С другой стороны, жесткая пена в основном используется в качестве строительного изоляционного материала..
Кроме того, пропиленоксид используется в производстве пропиленгликоля. Это соединение используется в производстве ненасыщенных полиэфирных смол и в качестве антифриза..
Кроме того, пропиленоксид используется в производстве простого эфира пропиленгликоля. Этот эфир имеет применение при производстве красок, одежды, чернил, смол и чистящих средств..
Для синтеза спиртов и других целей
Пропилен позволяет получать некоторые спирты, среди которых изопропанол, используемый в качестве растворителя в косметике и средствах личной гигиены. Кроме того, он выполняет функцию антисептика.
- Изопропанол участвует в производстве красок, смол, чернил и клейких лент. Он также используется в фармацевтической промышленности.
- Оксо-спирт-2-этилгексанол используется в производстве фталатов, пластификаторов, адгезивных материалов и красок..
- Бутанол используется в производстве красок, покрытий, смол, красителей, фармацевтических препаратов и полимеров..
С другой стороны, кумол производится из комбинации пропилена и бензола. Кумол является основным соединением в производстве фенола и ацетона, используемых в различных продуктах, таких как поликарбонаты, фенольные смолы, эпоксидные смолы и метилметакрилат..
Наконец, акриловая кислота - еще один продукт, полученный из пропилена, - используется в производстве сложных эфиров акриловой смолы и смол для красок, нанесения покрытий и нанесения клея..
ссылки
- Михал Осменда (26 декабря 2007 г.) Зажги мой огонь. [Рисунок]. Получено 23 мая 2018 г. с сайта commons.wikimedia.org
- Линде Групп. (2018). Пропилен. Получено 23 мая 2018 г. по адресу: linde-gas.com
- Wikipedia. (2018). Пропен. Получено 23 мая 2018 г. с сайта en.wikipedia.org
- PubChem. (2018). Пропилен. Получено 27 мая 2018 г. из: pubchem.ncbi.nlm.nih.gov
- Весович Велиса. (7 февраля 2011 г.) Пропилен. Получено 27 мая 2018 г. из: thermopedia.com
- Джеффри С. Плоткин. (8 августа 2016 г.) Пропиленовое затруднение. Получено 27 мая 2018 г. из: acs.org
- ICIS. (6 ноября 2017 г.) Использование пропилена и рыночные данные. Получено 27 мая 2018 г. из: icis.com


