Состав хлорида натрия (NaCl), свойства, применение, токсичность
хлорид натрия, также называемая поваренной солью или поваренной солью, представляет собой бинарную неорганическую соль натрия щелочного металла и галогена хлора. Это самый большой компонент пищевой соли, а его минеральная форма известна как галит. Молекулярная формула NaCl, и описывает стехиометрическое соотношение его ионов (Na+ Cl-), а не у дискретной молекулы (Na-Cl)
Хлорид натрия представляет собой кристаллическое белое твердое вещество, которое образуется в результате сочетания натрия, серебристо-белого металла, который бурно реагирует с водой, и элемента хлора, ядовитого, едкого, бледно-зеленого газа..

На верхнем изображении показана часть кристаллов NaCl. Как это возможно, что два элемента столь же опасны, как Na и Cl2, может образовываться пищевая соль? Во-первых, химическое уравнение его образования:
2Na (s) + Cl2(г) => 2NaCl (s)
Ответ заключается в природе ссылки в NaCl. Будучи ионным, свойства Na+ и Cl- они по диагонали отличаются от их нейтральных атомов.
Натрий является жизненно важным элементом, но в его ионной форме. На+ является основным внеклеточным катионом с концентрацией приблизительно 140 мг-экв / л, и вместе с сопровождающими его анионами Cl- и HCO3- (бикарбонат), в основном ответственны за величину осмолярности и внеклеточного объема.
Кроме того, Na+ отвечает за генерацию и проведение нервных импульсов в нейрональных аксонах, а также за инициацию сокращения мышц.
NaCl использовался с древних времен для придания аромата пище и сохранения мяса благодаря его способности уничтожать бактерии и предотвращать порчу.
Это также необходимо для производства гидроксида натрия (NaOH) и молекулярного хлора (Cl2) путем взаимодействия NaCl с водой при гидролизе:
2H2O (1) + 2 NaCl (s) => 2NaOH (ac) + Cl2(г) + Н2(G)
В катоде (-) Н накапливается2 (г) и NaOH. Между тем Cl накапливается на аноде (+)2 (G). Гидроксид натрия используется при производстве мыла и хлора при производстве пластика ПВХ.
индекс
- 1 Структура хлорида натрия
- 1.1 Унитарная ячейка
- 2 свойства
- 2.1 Молекулярная формула
- 2.2 Молекулярный вес
- 2.3 Физическое описание
- 2,4 Цвет
- 2.5 Вкус
- 2.6 Точка кипения
- 2.7 Точка плавления
- 2.8 Растворимость в воде
- 2.9 Растворимость в органических растворителях
- 2.10 Плотность
- 2.11 Давление пара
- 2.12 Стабильность
- 2.13 Разложение
- 2.14 Вязкость
- 2.15 Коррозия
- 2,16 рН
- 3 использования
- 3.1 В еду
- 3.2 Промышленное использование
- 3.3 Дома
- 3.4 Другое использование
- 3.5 Терапевтическое использование
- 4 Токсичность
- 4.1 Проглатывание
- 4.2 Раздражение и физический контакт
- 5 ссылок
Структура хлорида натрия
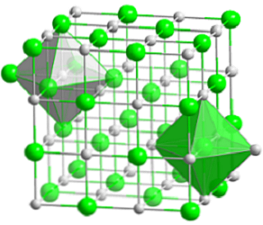
Компактная кубическая структура хлорида натрия представлена на верхнем рисунке. Объемные зеленые сферы соответствуют анионам Cl-, в то время как белый, к катионам Na+. Обратите внимание, что кристалл NaCl состоит из сети ионов, упорядоченных по электростатическим взаимодействиям в соотношении 1: 1..
Хотя столбцы показаны на изображении, связи не ковалентные, а ионные. Использование столбцов полезно при отображении координационной геометрии вокруг иона. Например, в случае NaCl каждый Na+ окружен шестью Cl- (белый октаэдр), и каждый Cl- из шести Na+ (зеленый октаэдр).
Следовательно, он имеет координацию (6,6), номера которой указывают, сколько соседей окружает каждый ион. Число справа указывает на соседей Na+, в то время как слева-.
Другие представления опускают использование полос, чтобы выделить октаэдрические отверстия, которые имеет структура, которые являются результатом межузельного пространства между шестью анионами Cl.- (или катионы Na+упаковано. Такое расположение наблюдается в других моно (MX) или многоатомных неорганических солях и называется солью драгоценного камня..
Унитарная ячейка
Элементарная ячейка каменной соли является кубической, но какие именно кубы точно представляют ее на изображении выше? Октаэдры дают ответ. Оба покрывают в общей сложности четыре маленьких кубика.
У этих кубиков есть части ионов в их вершинах, краях и гранях. Соблюдая осторожность, ион Na+ он расположен в центре и двенадцать из них по краям. Ион на одном ребре может быть разделен на четыре куба. Таким образом, есть 4 иона Na+ (12 × 1/4 + 1 = 4).
Для ионов Cl-, восемь расположены в вершинах и шесть по краям. Поскольку ионы, расположенные в вершинах, делят пространство с восемью другими кубами, а на краях с шестью, они имеют 4 иона Cl- (8 × 1/8 + 6 × 1/2 = 4).
Предыдущий результат интерпретируется следующим образом: в элементарной ячейке NaCl имеется четыре катиона Na+ и четыре Cl-аниона-; пропорция, которая соответствует химической формуле (Na+ для каждого Cl-).
свойства
Молекулярная формула
NaCl.
Молекулярный вес
58,44 г / моль.
Физическое описание
Кристаллическое твердое вещество.
цвет
Прозрачные бесцветные кристаллы или белый кристаллический порошок.
аромат
соленый.
Точка кипения
2,575 ºF до 760 мм рт.ст..
1,465 ºC.
Точка плавления
1474 ºF (800,7 ºC).
И температура кипения, и температура плавления отражают тепло, необходимое для преодоления кристаллической ретикулярной энергии. Следовательно, эти измерения подтверждают ионный характер NaCl.
Растворимость в воде
Больше или равно 100 мг / мл при 68 ° F.
36,0 г / 100 мл при 25 ºC.
На самом деле это гигроскопическая соль, которая удерживает влагу от окружающей среды..
Растворимость в органических растворителях
0,065 г / 100 мл этанола при 25 ° С; 10 г / 100 г глицерина при 25 ° С; 2,15 г / 100 мл жидкого аммония при 40 ° С; 1,4 г / 100 мл метанола при 25 ° С; 7,15 г / 100 этиленгликоля при 25 ° С и 5,21 г / 100 г муравьиной кислоты при 25 ° С.
плотность
2165 г / см3 при 77 ºC.
Давление пара
От 1 мм рт. Ст. До 1,589 ºF.
стабильность
Стабильно при рекомендуемых условиях хранения.
разложение
При нагревании до высоких температур разлагается с выделением паров соляной кислоты и оксида динатрия..
вязкость
Вязкость насыщенных растворов 1,93 мПа-с.
коррозия
Коррозийен для многих металлов.
pH
От 6,7 до 7,3 в водном растворе.
приложений
В еду
-Хлорид натрия использовался с древних времен для улучшения вкуса пищи и ее сохранения. Посол мяса - это способ уберечь его от бактериального действия, так как он задерживает разложение белка..
-С другой стороны, соль увеличивает осмолярность вокруг мяса, что вызывает поглощение осмосом воды бактерий, вызывая ее выведение.
Промышленное использование
Пищевая промышленность
-В пищевой промышленности соль используется в качестве усилителя вкуса, добавки для контроля ферментации, агента для контроля текстуры и проявителя цвета. Например, соль добавляют для выделения цвета в беконе, ветчине и других мясных продуктах..
-Соль служит связующим веществом при изготовлении колбас. Способствует образованию связующего геля, состоящего из мяса, жира и влаги.
-При обработке муки для выпечки хлеба во время варки добавляют соль, чтобы контролировать скорость брожения теста для хлеба. Он также используется для усиления глютена и в качестве усилителя вкуса, а также для начинки выпечки.
-Он используется в производстве сухих завтраков, смешанных или приготовленных мучных изделий, картофеля фри, кормов для собак и кошек и т. Д..
Синтез химических продуктов
-Хлорид натрия используется в качестве сырья при производстве гидроксида натрия и хлора, что, в свою очередь, полезно во многих химических отраслях промышленности..
-Соль используется при обработке различных металлов, например алюминия, меди, стали и ванадия. Это также используется, чтобы сделать хлорат натрия, который впоследствии используется в синтезе диоксида хлора, отбеливателя на основе кислорода. Диоксид хлора менее вреден для окружающей среды, чем другие отбеливатели.
В кожевенной промышленности
-Соль используется для подавления бактериального действия в коже, а также для ее регидратации..
В текстильной промышленности
-Соль используется в качестве протравы при крашении тканей. Используется для полоскания солевого раствора для удаления органических загрязнений и создания положительного заряда на поверхности тканей, что позволяет объединять отрицательно заряженные красители..
В нефтяной промышленности
-В разведке нефти и газа соль является важным компонентом буровых растворов. Он используется для флокуляции и увеличения плотности буровых растворов, что позволяет преодолевать высокие давления газа в скважинах, которые должны быть достигнуты. Кроме того, соль поддерживает насыщение бурового раствора.
-Соль помогает уплотнять почву, на которой строятся дороги. Уменьшает смещение, вызванное недрами в результате изменения влажности и автомобильного движения.
Дома
Соль использовалась втиранием при очистке поверхностей, кастрюль и сковородок. Также в профилактике плесени и как пятновыводитель. Также его используют во многих марках шампуня и зубной пасты..
Другое использование
На дорогах
-В ожидании снегопада дороги покрываются рассолом, что препятствует слипанию льда с поверхности дороги. Для размораживания используют смесь рассола и соли, а иногда добавляют другие химические компоненты, такие как хлориды магния или кальция. Использование соли и рассола не эффективно при температуре ниже -10ºC.
При добавлении соли наблюдается снижение криоскопической точки, коллигативного свойства растворов, которое каким-то образом препятствует образованию льда.
-Из-за своего гигроскопического состояния соль используется в качестве дешевого осушителя..
В смолах, используемых для умягчения воды
Жесткая вода содержит ионы кальция и магния, которые препятствуют действию мыла и производят отложения щелочных материалов в различном оборудовании и трубах. В умягчении воды используются ионообменные смолы. Соль используется при приготовлении и регенерации смол.
На огнетушителях
Хлорид натрия используется в огнетушителях для борьбы с пожарами, в которых присутствуют горючие металлы, такие как сплавы магния, калия, натрия и NK..
Соль действует как теплоотвод, а также как дробилка, которая ограничивает доступ кислорода к огню..
В очках
Кристаллы хлорида натрия используются в оптических компонентах, таких как окна и призмы, особенно для инфракрасного света. Однако, так как соль очень гигроскопична, происходит что-то вроде замерзания, которое покрывает линзы. По этой причине линзы из хлорида натрия были заменены линзами из селенида цинка (ZnSe)..
Терапевтическое использование
Восполнить недостаток солей в организме
-Когда есть истощение тела Na+, должны быть заменены для поддержания внеклеточной осмолярности, нервной проводимости и сокращения мышц.
-NaCl используется для лечения и профилактики дефицита натрия и хлора в результате чрезмерного потоотделения при воздействии высоких температур. Он также используется при чрезмерном диурезе или чрезмерном ограничении потребления соли.
-Парентеральная доставка 045% раствора NaCl используется для лечения гиперосмолярного диабета. Он выполняет регидратирующую функцию и служит для оценки состояния почечной функции..
-Инъекции гипертонических растворов с концентрацией NaCl более 0,9% мас. / Об.,
-Они используются при сильном истощении Na+, будучи восстановлением необходимого иона. Эта гипонатриемия может быть следствием лечения свободными электролитами или концентрацией Na+.
Гипонатриемия также может быть вызвана чрезмерным потреблением воды, не контролируемой недостаточной функцией почек..
В лечении и нетрадиционном использовании
-Растворы для ингаляции NaCl используются для разбавления лекарств, используемых в процессе распыления. Он также используется для промывания трахеи и орошения. 0,9% физиологический раствор, используемый в назальных спреях.
-20% -ные растворы NaCl используются для внутриамниотической трансабдоминальной установки, таким образом вызывая поздний аборт во втором триместре беременности.
-Хлорид натрия можно использовать как местный антисептик. Благодаря своей осмотической способности он способен обезвоживать широкий спектр вирусов и бактерий в несгоревшем состоянии; следовательно, он используется в качестве болезненного антисептика для дезинфекции ран.
токсичность
прием пищи
Он оказывает вредное влияние на здоровье только в том случае, если потребление высокое и длительное время. При этих обстоятельствах гипернатриемия может возникнуть с последующим увеличением внеклеточного объема, что приведет к повышению артериального давления.
Раздражение и физический контакт
Он оказывает токсическое действие, только если вдыхание очень велико. При попадании на кожу в чрезмерном виде может вызвать ее сухость. Наконец, это вызывает кратковременное раздражение при контакте с глазами.
ссылки
- Дрожь и Аткинс. (2008). Неорганическая химия (Четвертое издание, стр. 84, 90, 93, 263). Mc Graw Hill.
- Уиттен, Дэвис, Пек и Стэнли. Химия. (8-е изд.). CENGAGE Learning, стр. 482-483.
- Хлорид натрия (2018). Хлорид натрия: преимущества, использование, свойства, риски. Взято из: clorurodesodio.org
- PubChem. (2018). Хлорид натрия. Получено из: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2018). Хлорид натрия. Взято из: en.wikipedia.org
- Американские элементы. (2018). Хлорид натрия. Взято из: americanelements.com


