Формула осмолярности, как ее вычислить и разница с осмоляльностью
осмолярность является параметром, который измеряет концентрацию химического соединения в литре раствора, если он способствует коллигативному свойству, известному как осмотическое давление указанного раствора.
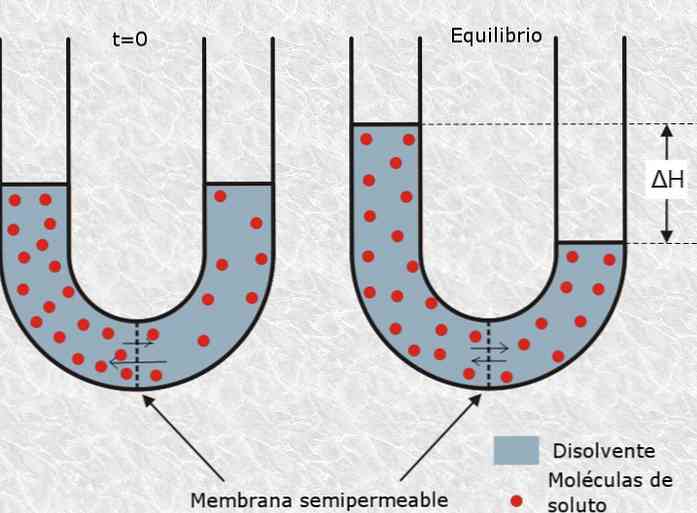
В этом смысле осмотическое давление раствора относится к количеству давления, необходимому для замедления процесса осмоса, которое определяется как избирательное прохождение частиц растворителя посредством полупроницаемой или пористой мембраны из раствора. от более низкой концентрации к более концентрированной.
Кроме того, единицей измерения количества растворенных частиц является осмол (символом которого является Осм), который не является частью Международной системы единиц (СИ), используемой почти во всем мире. Поэтому концентрация растворенного вещества в растворе определяется в единицах осмолей на литр (Осм / л).
индекс
- 1 Формула
- 1.1 Определение переменных в формуле осмолярности
- 2 Как рассчитать?
- 3 Различия между осмолярностью и осмоляльностью
- 4 Ссылки
формула
Как упоминалось ранее, осмолярность (также известная как осмотическая концентрация) выражается в единицах, определенных как осм / л. Это связано с его взаимосвязью с определением осмотического давления и измерением диффузии растворителя с помощью осмоса..
На практике осмотическая концентрация может быть определена как физическая величина с использованием осмометра..
Осмометр - это инструмент, используемый для измерения осмотического давления раствора, а также для определения других коллигативных свойств (таких как давление пара, повышение температуры кипения или снижение температуры замерзания) для получения значения осмолярности раствора.
Таким образом, для расчета этого параметра измерения используется следующая формула, которая учитывает все факторы, которые могут повлиять на это свойство..
Осмолярность = ΣφЯNЯСЯ
В этом уравнении осмолярность определяется как сумма, полученная в результате умножения всех значений, полученных по трем различным параметрам, которые будут определены ниже..
Определение переменных в формуле осмолярности
Во-первых, это осмотический коэффициент, представленный греческой буквой φ (фи), который объясняет, как далеко удаляется решение идеального поведения, или, другими словами, степень неидеальности, которую растворенное вещество проявляет в решении.
Проще всего, φ относится к степени диссоциации растворенного вещества, которая может иметь значение от нуля до единицы, где максимальное значение единицы представляет собой диссоциацию 100%; то есть абсолют.
В некоторых случаях, таких как сахароза, эта величина превышает единицу; в то время как в других случаях, таких как влияние солей, влияние электростатических взаимодействий или сил вызывает осмотический коэффициент со значением, меньшим единицы, даже если происходит абсолютная диссоциация.
С другой стороны, значение n указывает количество частиц, в которых молекула может быть диссоциирована. В случае ионных частиц в качестве примера приведен хлорид натрия (NaCl), значение n которого равно двум; тогда как в неионизированной молекуле глюкозы значение n равно единице.
Наконец, значение с представляет концентрацию растворенного вещества, выраженную в мольных единицах; и нижний индекс i относится к идентичности конкретного растворенного вещества, но он должен быть одинаковым при умножении трех факторов, упомянутых выше, и, таким образом, получении осмолярности.
Как рассчитать?
В случае ионного соединения KBr (известного как бромид калия), если у вас есть раствор с концентрацией, равной 1 моль / л KBr в воде, предполагается, что он имеет осмолярность, равную 2 осмоль / л..
Это связано с его сильным электролитным характером, что способствует его полной диссоциации в воде и позволяет высвобождению двух независимых ионов (K+ и Br-), которые имеют некоторый электрический заряд, так что каждый моль KBr равен двум осмолам в растворе.
Аналогично для раствора с концентрацией, равной 1 моль / л BaCl2 (известный как хлорид бария) в воде, он имеет осмолярность, равную 3 осмоль / л.
Это связано с тем, что выделяются три независимых иона: ион Ва2+ и два иона Cl-. Затем каждый моль BaCl2 эквивалентно трем осмолам в растворе.
С другой стороны, неионные вещества не подвергаются такой диссоциации и генерируют один осмол на каждый моль растворенного вещества. В случае раствора глюкозы с концентрацией, равной 1 моль / л, это равняется 1 осмоль / л раствора.
Различия между осмолярностью и осмоляльностью
Осмол определяется как количество частиц, которые растворяются в объеме, равном 22,4 л растворителя, при температуре 0 ° С и которые вызывают образование осмотического давления, равного 1 атм. Следует отметить, что эти частицы считаются осмотически активными.
В этом смысле свойства, известные как осмолярность и осмоляльность, относятся к одному и тому же измерению: концентрация растворенного вещества в растворе или, другими словами, содержание общих частиц растворенного вещества в растворе..
Принципиальное различие, которое установлено между осмолярностью и осмоляльностью, заключается в единицах, в которых каждый представлен:
Осмолярность выражается в количестве вещества на объем раствора (то есть, осмоль / л), тогда как осмолярность выражается в количестве вещества на массу растворителя (то есть, осмоль / кг раствора)..
На практике оба параметра используются безразлично, даже проявляя себя в разных единицах, из-за того, что между суммарными величинами разных измерений существует незначительная разница.
ссылки
- Wikipedia. (Н.Д.). Осмотическая концентрация. Получено с es.wikipedia.org
- Чанг, Р. (2007). Химия, девятое издание. Мексика: Макгроу-Хилл.
- Эванс, Д. Х. (2008). Осмотическая и ионная регуляция: клетки и животные. Получено из books.google.co.ve
- Potts, W. T. и Parry, W. (2016). Осмотическая и ионная регуляция у животных. Получено из books.google.co.ve
- Армитаж, К. (2012). Исследования по общей биологии. Получено из books.google.co.ve


